중대성과 시급성에 따라 ‘1개월’ 또는 ‘3개월’ 차등 적용
식품의약품안전처는 의약품 허가사항이 변경될 경우 첨부문서(라벨) 교체에 필요한 유예기간을 현행 ‘1개월’에서 ‘최대 3개월’까지로 연장한다고 밝혔다.
현재 △재심사 △안전성 정보처리 △안전성·유효성 심사결과 등 허가사항을 변경 지시한 경우 신속한 정보 전달을 위해 1개월 내에 첨부문서를 바꾸도록 명시하고 있다.
식약처는 이번 연장은 업계의 건의사항에 따라 일괄적으로 적용해왔던 변경 유예기간(1개월)을 중대성과 시급성에 따라 유예기간을 ‘1개월’과 ‘3개월’로 차등 적용하기로 한 것이라고 설명했다.
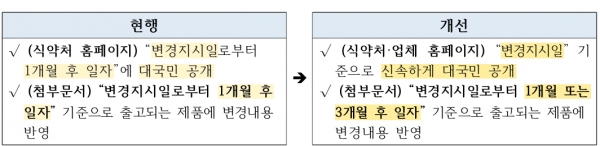
구체적으로 안전성을 이유로 효능·효과, 용법·용량 제한, 사용상의 주의사항 중 ‘경고’ 또는 ‘금기’ 변경, 그 밖에 중대성·시급성이 요구되는 정보는 유예기간을 지금처럼 1개월로 적용하고, 그 외 정보는 3개월을 적용하기로 했다 .
식약처는 특히 국민의 알 권리 강화를 위해 변경지시일로부터 1개월 후에 변경된 사항을 식약처 홈페이지에 공개하도록 했던 것을 변경지시일 기준으로 가능한 신속하게 업체 홈페이지에도 게재하도록 했다고 말했다.
식약처 관계자는 “업계의 애로사항을 해소하고 부담을 완하할 수 있는 정책 방향을 모색해 지속적으로 개선하겠다”고 밝혔다.
저작권자 © 의사신문 무단전재 및 재배포 금지


