현재 국내에서 코로나19 백신·치료제 24개 제품 임상 진행 중
국내에서 개발 중인 코로나19 백신의 임상시험계획이 보건당국으로부터 승인을 받았다.
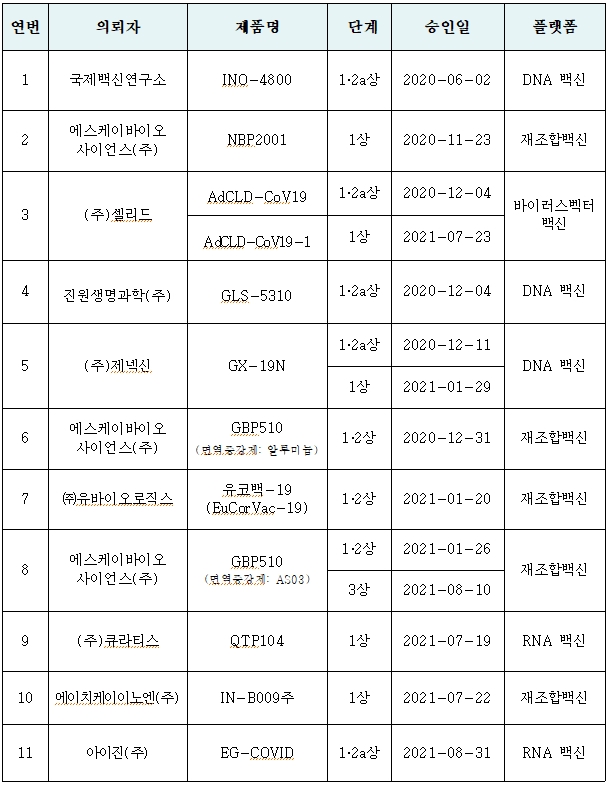
이로써 국내에서 코로나19 관련해 임상시험을 진행하고 있는 의약품은 백신 11개, 치료제 13개(12개 성분) 등 총 24개 제품이 됐다.
식품의약품안전처(처장 김강립)는 아이진이 개발 중인 코로나19 백신 후보물질 ‘EG-COVID’의 안전성과 면역원성을 평가하기 위한 임상 1·2a상시험계획을 31일 승인했다고 밝혔다.
면역원성은 바이러스 감염성을 없애거나 낮추는 ‘중화항체’ 증가 비율을 말한다. 또 임상 1·2a상시험은 1·2a상을 동시에 승인, 1상에서 안전성 등을 확인하고 순차적으로 2a상을 진행하는 것이다.
‘EG-COVID’는 코로나19 바이러스의 ‘표면항원 단백질’ 정보를 담고 있는 mRNA 백신으로, mRNA의 세포 내 전달을 위한 물질로 인지질과 콜레스테롤 등으로 만든 미세한 원형의 이중막인 리포솜(liposome)을 사용했다.
이 백신은 코로나19 바이러스 항원 정보를 가진 유전자를 mRNA 형태로 주입해 체내에서 항원 단백질을 합성하고, 이 항원 단백질이 면역세포를 자극해 중화항체 생성을 유도하며, 바이러스가 인체에 침입했을 때 바이러스를 중화해 제거하게 된다.
식약처 관계자는 “앞으로도 국민적 관심이 높은 코로나19 치료제·백신 개발 제품의 임상시험 현황에 대한 정보를 신속하게 전달하겠다”며 “안전하고 효과 있는 코로나19 치료제·백신 개발을 지원하겠다”고 말했다.

저작권자 © 의사신문 무단전재 및 재배포 금지


