국내선 치료제 19건, 백신 2건 시험중···“’항체치료제’ 개발속도 가장 빨라”

정부가 글로벌 제약사 화이자가 개발중인 코로나19 백신에 대해 최종 임상 결과까지 신중히 지켜보는 것을 전제로 국내 도입을 논의하겠다고 밝혔다. 화이자의 글로벌 임상 3상 시험 중간 결과에서 접종자 94명 중 90%이상에서 코로나 예방 효과가 나온 데 따른 것이다.
식품의약품안전처는 10일 정례브리핑을 통해 현재 국내에서 개발되고 있는 코로나19 치료제 및 백신의 임상시험 및 허가·심사 현황에 대해 설명했다.
서경원 식약처 의약품심사부장은 “화이자가 개발중인 코로나 백신 결과는 8일 기준 3만 8,599명이 2번 접종을 받고 그 중에서 감염자가 94명이 나온 시점에서 중간분석을 한 결과를 발표한 것”이라며 “백신을 맞지 않은 군과 비교를 했을 때 백신을 맞은 군에서 예방효과가 90% 이상 나왔다”고 설명했다
이어 “중간결과는 긍정적으로 보이지만, 최종 임상결과를 종합적으로 보고 효과, 안전성, 면역력 지속기간, 또 고령자에 대한 효과 등을 판단할 수 있을 것이라 생각한다”며 “면밀하게 모니터링을 하고 정부 차원에서도 도입을 위해서 논의를 할 예정”이라고 밝혔다.
권준욱 중앙방역대책본부 부본부장 역시 "9개월 만에 임상 3상을 통해서 좋은 결과가 나온 것은 사례를 또 찾기 어려울 정도로 매우 좋은 상황임에는 틀림이 없지만 개발 이상으로 더 중요한 것이 실제로 도입하고 접종하며 이상반응을 모니터링 등을 진행하는 것”이라며 “앞선 나라들의 부작용을 천천히 살펴보면서 국내 전문가들과 함께 접종 전략을 수정·보완하겠다. 무엇보다 (백신 공급에 앞서 유통을 위한)콜드체인과 시스템을 완비해야 한다”고 강조했다.
한편, 식약처에 따르면 국내에서 승인한 임상시험은 치료제 26건, 백신 2건으로 현재 진행 중인 임상시험은 치료제 19건 백신 2건으로 총 21건이다. 이 중 개발 속도가 가장 빠른 것은 ‘항체치료제’다.
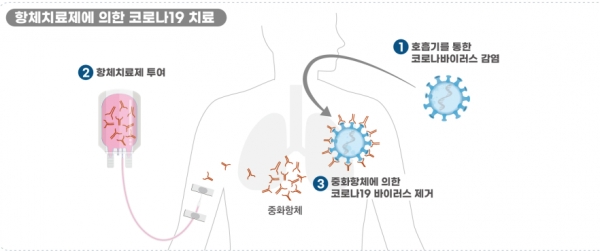
현재, 국내에서 개발되고 있는 항체치료제로 셀트리온의 제품이 코로나19 경증~중등증 환자를 대상으로 2/3상 임상시험을 다국가 임상으로 진행하고 있는 것으로 나타났다.
또한, 해외에서 개발되고 있는 항체치료제로 미국의 릴리社와 리제네론社의 제품이 코로나19 경증~중등증 환자를 대상으로 2/3상 임상시험을 진행 중이다. 두 제품은 모두 지난달 7일 미국 FDA에 긴급사용승인을 신청했고 릴리社의 항체치료제의 경우 9일 승인을 받은 것으로 알려졌다.


